Fontes: https://mundoeducacao.uol.com.br/quimica/lei-conservacao-massa.htm
https://brasilescola.uol.com.br/quimica/lei-proust-ou-lei-das-proporcoes-constantes.htm
Com isso, ele enunciou a Lei de Conservação da Massa da seguinte forma:
“No interior de um recipiente fechado, a massa total não varia, quaisquer que sejam as transformações que venham a ocorrer.”
Ou
“Num recipiente fechado, a soma das massas dos reagentes é igual à soma das massas dos produtos.”
Atualmente, essa lei é mais conhecida pelo seguinte enunciado:
“Na natureza, nada se perde, nada se cria, tudo se transforma.”

A lei de conservação das massas foi criada por Lavoisier
O químico francês Joseph Louis Proust (1754-1826) passou a realizar cuidadosas experiências relacionando as massas dos componentes de determinadas reações.
Por exemplo, os elementos que compõem a água são o hidrogênio e o oxigênio. Proust verificou que nessa reação de formação da água, o hidrogênio sempre reagia com o oxigênio em uma proporção constante e definida, que era de 1:8, respectivamente. Veja como isso ocorre abaixo:
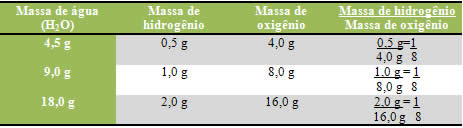
Observe que não importa a quantidade de massa dos elementos usada, a proporção sempre será a mesma.
Proust observou que isso não ocorria somente com a água, mas com todas as outras substâncias.
São formados 15,06 g de sulfeto cúprico (CuS), por exemplo, reagindo 10,00 g de cobre metálico (Cu) com 5,06 g de enxofre (S). Assim, se dobrarmos a quantidade de cobre (que irá para 20,0 g), e se quisermos que todo o cobre reaja, será necessário dobrar também a quantidade do enxofre, para 10,12 g, com a formação total de 30,12 g de sulfeto.
Agora, se for colocada uma quantidade que não esteja em proporção, a quantidade em excesso irá sobrar, não irá reagir. Observe isso a seguir:
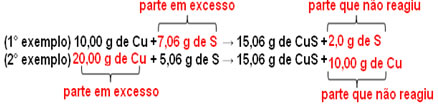
Observe que a reação só ocorre de acordo com a proporção definida. Por isso, em 1799, Proust concluiu que, quando várias substâncias se combinam para formar um composto, isso é sempre feito numa relação de massas definida.
As reações químicas são processos que transformam uma ou mais substâncias, chamados reagentes, em outras substâncias, chamadas produtos. Em uma linguagem mais acadêmica, dizemos que uma reação química promove mudança na estrutura da matéria.
Na química inorgânica podemos classificar as reações em quatro tipos diferentes:
1) Reações de síntese ou adição
As reações de síntese ou adição são aquelas onde substâncias se juntam formando uma única substância. Representando genericamente os reagentes por A e B, uma reação de síntese pode ser escrita como:
Veja alguns exemplos:
Fe + S  FeS
FeS
2H2 + O2  2H2O
2H2O
H2O + CO2  H2CO3
H2CO3
Perceba nos exemplos que os reagentes não precisam ser necessariamente substâncias simples (Fe, S, H2, O2), podendo também ser substâncias compostas (CO2, H2O) mas, em todas elas o produto é uma substância "menos simples" que as que o originaram.
2) Reações de análise ou decomposição
As reações de análise ou decomposição são o oposto das reações de síntese, ou seja, um reagente dá origem a produtos mais simples que ele. Escrevendo a reação genérica fica fácil entender o que acontece:
Não parece bastante simples? E é bastante simples. Veja nos exemplos:
2H2O  2 H2 + O2
2 H2 + O2
2H2O2  2H2O + O2
2H2O + O2
Reversibilidade das reações químicas
Os exemplos podem sugerir que qualquer reação de síntese pode ser invertida através de uma reação de análise. Isso não é verdade. Algumas reações podem ser reversíveis, como podemos notar na reação da água:
2H2 + O2  2H2O
2H2O
2H2O  2H2 + O2
2H2 + O2
Entretanto, isso não é uma regra.
3) Reações de deslocamento
As reações de deslocamento ou de simples-troca merecem um pouco mais de atenção do que as anteriores. Não que sejam complicadas, pois não são, mas por alguns pequenos detalhes. Em sua forma genérica ela pode ser escrita como:
Vamos entender o que aconteceu: C trocou de lugar A. Simples assim, mas será que isso ocorre sempre? É intuitivo que não. Iamgine o seguinte: você entra em um baile e vê a pessoa com quem gostaria de dançar dançando com outra pessoa. Você vai até lá e tentará fazê-la mudar de par, ou seja, estará tentando deslocar o acompanhante indesejável e assumir seu lugar. Se você for mais forte que o "indesejável", basta dar-lhe um empurrão e assumir seu lugar mas, se ele for um brutamontes troglodita, possivelmente ele nem sentirá seu empurrão. Na reação de deslocamento o processo é idêntico: C vê B ligado a A, aproxima-se e, sendo mais forte, desloca A e assume a ligação com B. Caso C não seja mais forte que A nada acontece.
Basta então saber que é mais forte que quem:
Desta forma, temos:
2Na + 2H2O  2NaOH + H2 (o sódio desloca o hidrogênio da água H-OH)
2NaOH + H2 (o sódio desloca o hidrogênio da água H-OH)
Au + HCl  não reage (o ouro não consegue deslocar o hidrogênio)
não reage (o ouro não consegue deslocar o hidrogênio)
4) Reações de dupla-troca
São também muito simples, mas devemos também ficar atento a detalhes. O mecanismo é fácil:
Certamente você já percebeu o que aconteceu: A trocou de lugar com C. A diferença desse tipo com as de deslocamento é que nem A nem C estavam sozinhos e, após a troca nenhum deles ficou sozinho.
Para entendermos como e quando uma reação deste tipo ocorre teremos que observar o seguinte:
- A substância AB está em solução e, desta forma, o que temos na verdade são os íons A+ e B- separados uns dos outros. A substância CD também está em solução, portanto temos também os íons C+ e D- separados;
- Quando juntamos as duas soluções estamos promovendo uma grande mistura entre os íons A+, B-, C+ e D-, formando uma grande "sopa de íons";
- Se, ao combinarmos C+ com B-, o composto CB for solúvel, os íons serão novamente separados em C+ e B-, resultando exatamente na mesma coisa que tínhamos anteriormente. O mesmo acontece com A+ e B-.
Assim, ao misturarmos AB com CD, estamos na verdade fazendo:
E perceba que juntar íons que se separarão novamente resultará na mesma "sopa de íons" e não resultará em nenhuma nova substância, portanto não ocorre nenhuma reação.
Para que a reação efetivamente ocorra, será necessário que ao menos um dos prováveis produtos (AD ou CB) não sejam separados ao se juntarem, ou seja, deve-se formar um composto insolúvel e isso é conseguido através de um sal insolúvel, de um gás ou de água. Se um dos produtos for um sal insolúvel ele não será separado em ións e permanecerá sólido. Se for um gás ele se desprenderá da solução (borbulhas) e também permanecerá com suas moléculas agrupadas. Se um dos produtos for a água, ela não se desagrupa em sua própria presença.
NaCl + AgNO3  NaNO3 + AgCl
NaNO3 + AgCl
Nesta reação o produto AgCl (cloreto de prata) é insolúvel, portanto a reação ocorre.
NaCl + LiNO3  NaNO3 + LiCl
NaNO3 + LiCl
Como nenhum dos produtos formados, NaNO3 (nitrato de sódio) ou LiCl (cloreto de lítio) é insolúvel, a reação não ocorre
NaOH + HCl  NaCl + H2O
NaCl + H2O
Como um dos produtos é a água (H2O), a reação ocorre.
Para a previsão da ocorrência ou não de uma reação de dupla-troca é fundamental que conheçamos a solubilidade dos sais em água e, para relembrar isso, leia o texto sobre solubilidade em água.
Viu como é simples? Com um pouco de prática e exercícios você consegue até escrever reações que podem dar origem a um determinado produto. Quer ver?
Imagine que você que obter sulfato de chumbo (PbSO4) . Você sabe que terá que juntar o íon chumbo (Pb2+) e o íon sulfato (SO42-). Como você sabe que o sulfato de chumbo é insolúvel, pode promover uma dupla-troca:
PbX + YSO4  PbSO4 + XY
PbSO4 + XY
É só escolher X e Y de forma que as duas substâncias sejam solúveis.
Outra forma é fazer um deslocamento do hidrogênio pelo chumbo, já que este é mais reativo:
Pb + H2SO4  H2 + PbSO4
H2 + PbSO4
Não falei que era fácil?






Comentários
Postar um comentário